CELLULAR NEIGHBORHOODS: THE NEW PHENOTYPE / VICINI CELLULARI: IL NUOVO FENOTIPO
CELLULAR NEIGHBORHOODS: THE NEW PHENOTYPE. The process of the ENEA patent RM2012A000637 is very useful in this type of application./ VICINI CELLULARI: IL NUOVO FENOTIPO. Il procedimento del brevetto ENEA RM2012A000637 è molto utile in questotipo di applicazione.
Segnalato dal Dott. Giuseppe Cotellessa / Reported by Dr. Giuseppe Cotellessa
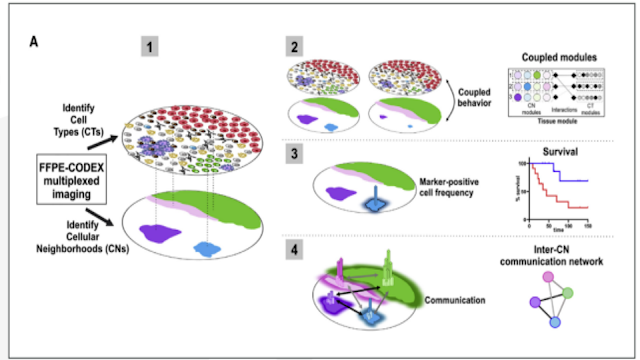
FIGURE 11: Conceptual framework for CN mapping combining cell type as identified by label with the known composition and morphology of the tissue. Source: Schürch, CM et al. Coordinated cellular neighborhoods orchestrate antitumoral immunity at the colorectal cancer invasive front. / Quadro concettuale per la mappatura CN che combina il tipo di cellula identificato dall'etichetta con la composizione e la morfologia note del tessuto. Fonte: Schürch, CM et al. Quartieri cellulari coordinati orchestrano l'immunità antitumorale sul fronte invasivo del cancro del colon-retto.
The concept of neighborhoods quickly came to the fore, because we were seeing multiple groupings of cells that would repeat across a tissue, and these groupings would correlate with observations that pathologists have been making for 50 years.
One result of seeing where every cell sits in the tissue labeled to reveal its specific function and phenotype is that patterns begin to emerge that align with particular pathologies or outcomes. Dr. Garry Nolan, a leading expert in spatial biology and Professor of Microbiology and Immunology at Stanford University, refers to these tissue structures as “cellular neighborhoods.” Nolan’s lab demonstrated the utility of the neighborhood concept in colorectal cancer (CRC), where they sought to explain how the roles of different cell types change based on their position within the immune tumor microenvironment (iTME). To do this, they identified two different CRC patient groups with significantly different prognostic outcomes. One cohort’s iTME was characterized by numerous tertiary lymphoid structures (TLS) and labeled as CLR for “Crohns-like reaction.” The group with the higher mortality rates was characterized by diffuse inflammatory infiltration (DII) but low TLS formation. It was labeled DII. For both groups, they used multiplexed tissue imaging to identify cellular neighborhoods (CNs) based on cellular composition and morphology (FIGURE 11).
The hypothesis was that the difference in survival between the two groups was likely influenced by differences in their antitumoral immune response as opposed to tumor intrinsic factors, and this was borne out by the neighborhood mapping process. The research focused on nine cellular neighborhoods that recapitulated core tissue components such as T-cell enriched (CN1), bulk tumor (CN2), macrophage enriched (CN4), tumor FIGURE 12: Table B (left) lists the nine cellular neighborhoods identified in the colorectal cancer cells, and the cell types present in each. The maps on the right illustrate the difference in the relatively well-delineated neighborhoods in CLR patients and the highly intermixed neighborhood structures associated with poorer survival in DII patients. Source: Schürch, CM et al. Coordinated cellular neighborhoods orchestrate antitumoral immunity at the colorectal cancer invasive front. Cell. 2020 Sept 03; 182, p 1348.
https://doi.org/10.1016/j.cell.2020.07.005 boundary (CN6), and granulocyte enriched (CN9) (FIGURE 12). They found that the cellular composition of the different neighborhoods shifted between patients in the DII and CLR groups, and that disease prognosis in either group could be linked to specific intra-neighborhood interactions and changes in the cellular mix within neighborhoods.
FIGURE 12: Table B (left) lists the nine cellular neighborhoods identified in the colorectal cancer cells, and the cell types present in each. The maps on the right illustrate the difference in the relatively well-delineated neighborhoods in CLR patients and the highly intermixed neighborhood structures associated with poorer survival in DII patients. Source: Schürch, CM et al. Coordinated cellular neighborhoods orchestrate antitumoral immunity at the colorectal cancer invasive front. / La tabella B (a sinistra) elenca i nove quartieri cellulari identificati nelle cellule tumorali del colon-retto e i tipi di cellule presenti in ciascuno di essi. Le mappe a destra illustrano la differenza nei quartieri relativamente ben delineati nei pazienti CLR e le strutture di quartiere altamente mescolate associate a una sopravvivenza più scarsa nei pazienti DII. Fonte: Schürch, CM et al. Quartieri cellulari coordinati orchestrano l'immunità antitumorale sul fronte invasivo del cancro del colon-retto
FIGURE 13: Neighborhood structures in CLR patients are compartmentalized with a separate “tumor compartment” and “immune compartment,” while in DII patients, tumor and immune compartments were mixed. The separate compartments correlate with a higher survival rate, suggesting that tumor cells may interfere with anti-tumor effects of immune cells in the mixed model. Source: Schürch, CM et al. Coordinated cellular neighborhoods orchestrate antitumoral immunity at the colorectal cancer invasive front. / Le strutture dei vicini nei pazienti con CLR sono compartimentalizzate con un "compartimento tumorale" e un "compartimento immunitario" separati, mentre nei pazienti DII, i compartimenti tumorali e immunitari erano mescolati. I compartimenti separati sono correlati ad un tasso di sopravvivenza più elevato, suggerendo che le cellule tumorali possono interferire con gli effetti antitumorali delle cellule immunitarie nel modello misto. Fonte: Schürch, CM et al. Quartieri cellulari coordinati orchestrano l'immunità antitumorale sul fronte invasivo del cancro del colon-retto.
It all comes back to a simple idea that the same immune cell placed in a different context within the tumor can play a completely different role.
In CLR patients the neighborhoods constituted a separate “immune compartment” and “tumor compartment,” which correlated with higher survival rates (FIGURE 13). By contrast, in DII patients the tumor and immune modules were combined in a single compartment, suggesting that in DII patients the tumor may interfere with or regulate anti-tumor immune processes. Notably, survival was higher in DII patients where there was a robust CD9 granulocyte neighborhood with elevated levels of PD-1+ and CD4+ T cells. While these observations correlate with existing assumptions about the predictive value of TLS levels and CD4:CD8 ratios, this research for the first time showed how these relationships were tied to finer cell and protein interactions captured by the neighborhood model.
ITALIANO
Il concetto di quartieri è venuto rapidamente alla ribalta, perché stavamo vedendo più raggruppamenti di cellule che si sarebbero ripetuti in un tessuto e questi raggruppamenti sarebbero stati correlati alle osservazioni che i patologi hanno fatto per 50 anni.
Un risultato del vedere dove ogni cellula si trova nel tessuto etichettato per rivelare la sua specifica funzione e fenotipo è che iniziano a emergere modelli che si allineano con particolari patologie o esiti. Il dottor Garry Nolan, uno dei massimi esperti di biologia spaziale e professore di microbiologia e immunologia presso la Stanford University, si riferisce a queste strutture tissutali come "quartieri cellulari". Il laboratorio di Nolan ha dimostrato l'utilità del concetto di quartiere nel cancro del colon-retto (CRC), dove hanno cercato di spiegare come i ruoli dei diversi tipi di cellule cambiano in base alla loro posizione all'interno del microambiente tumorale immunitario (iTME). Per fare ciò, hanno identificato due diversi gruppi di pazienti con CRC con esiti prognostici significativamente diversi. L'iTME di una coorte era caratterizzata da numerose strutture linfoidi terziarie (TLS) ed etichettata come CLR per "reazione simile a Crohns". Il gruppo con i tassi di mortalità più elevati era caratterizzato da infiltrazione infiammatoria diffusa (DII) ma bassa formazione di TLS. Era etichettato DII. Per entrambi i gruppi, hanno utilizzato l'imaging tissutale multiplexato per identificare i quartieri cellulari (CN) in base alla composizione cellulare e alla morfologia (FIGURA 11).
L'ipotesi era che la differenza di sopravvivenza tra i due gruppi fosse probabilmente influenzata dalle differenze nella loro risposta immunitaria antitumorale rispetto ai fattori intrinseci del tumore, e questo è stato confermato dal processo di mappatura del vicinato. La ricerca si è concentrata su nove quartieri cellulari che ricapitolavano componenti del tessuto centrale come l'arricchimento di cellule T (CN1), il tumore di massa (CN2), l'arricchimento di macrofagi (CN4), il tumore FIGURA 12: la tabella B (a sinistra) elenca i nove quartieri cellulari identificati in le cellule tumorali del colon-retto e i tipi di cellule presenti in ciascuna di esse. Le mappe a destra illustrano la differenza nei quartieri relativamente ben delineati nei pazienti CLR e le strutture di quartiere altamente mescolate associate a una sopravvivenza più scarsa nei pazienti DII. Fonte: Schürch, CM et al. Quartieri cellulari coordinati orchestrano l'immunità antitumorale sul fronte invasivo del cancro del colon-retto. Cellula. 03 settembre 2020; 182, p 1348. https://doi.org/10.1016/j.cell.2020.07.005 confine (CN6) e arricchimento di granulociti (CN9) (FIGURA 12). Hanno scoperto che la composizione cellulare dei diversi quartieri variava tra i pazienti nei gruppi DII e CLR e che la prognosi della malattia in entrambi i gruppi poteva essere collegata a specifiche interazioni intra-quartiere e cambiamenti nel mix cellulare all'interno dei quartieri.
Tutto torna alla semplice idea che la stessa cellula immunitaria collocata in un contesto diverso all'interno del tumore possa svolgere un ruolo completamente diverso.
Nei pazienti con CLR i quartieri costituivano un "compartimento immunitario" e un "compartimento tumorale" separati, correlati a tassi di sopravvivenza più elevati (FIGURA 13). Al contrario, nei pazienti DII il tumore ed i moduli immunitari sono stati combinati in un unico compartimento, suggerendo che nei pazienti DII il tumore può interferire con o regolare i processi immunitari antitumorali. In particolare, la sopravvivenza era più alta nei pazienti DII dove c'era un robusto quartiere di granulociti CD9 con livelli elevati di cellule T PD-1+ e CD4+. Sebbene queste osservazioni siano correlate con le ipotesi esistenti sul valore predittivo dei livelli di TLS e dei rapporti CD4: CD8, questa ricerca ha mostrato per la prima volta come queste relazioni fossero legate ad interazioni cellulari e proteiche più fini catturate dal modello di vicinato.
Da:
https://547446.fs1.hubspotusercontent-na1.net/hubfs/547446/Technology%20Networks/Landing%20Pages/Akoyabio/Phenocycler_White-Paper_How-Spatial-Phenotyping-Can-Uncover-Novel-Insights-in-Tissue-Biology.pdf?__hstc=8807082.f01d3c6596a65dcef4221e29cb9c3403.1626181017248.1675854152534.1675870217673.1931&__hssc=8807082.8.1675870217673&__hsfp=1734902676





Commenti
Posta un commento