Gas Chromatography – How a Gas Chromatography Machine Works, How To Read a Chromatograph and GCxGC / Gascromatografia - Come funziona una macchina per gascromatografia, Come leggere un cromatografo e GCxGC
Gas Chromatography – How a Gas Chromatography Machine Works, How To Read a Chromatograph and GCxGC / Gascromatografia - Come funziona una macchina per gascromatografia, Come leggere un cromatografo e GCxGC
Segnalato dal Dott. Giuseppe Cotellessa / Reported by Dr. Giuseppe Cotellessa

What is gas chromatography?
Gas chromatography (GC) is an analytical technique used to separate the chemical components of a sample mixture and then detect them to determine their presence or absence and/or how much is present. These chemical components are usually organic molecules or gases. For GC to be successful in their analysis, these components need to be volatile, usually with a molecular weight below 1250 Da, and thermally stable so they don’t degrade in the GC system. GC is a widely used technique across most industries: for quality control in the manufacture of many products from cars to chemicals to pharmaceuticals; for research purposes from the analysis of meteorites to natural products; and for safety from environmental to food to forensics. Gas chromatographs are frequently hyphenated to mass spectrometers (GC-MS) to enable the identification of the chemical components.
How does gas chromatography work?
As the name implies, GC uses a carrier gas in the separation, this plays the part of the mobile phase (Figure 1 (1)). The carrier gas transports the sample molecules through the GC system, ideally without reacting with the sample or damaging the instrument components.
The sample is first introduced into the gas chromatograph (GC), either with a syringe or transferred from an autosampler (Figure 1 (2)) that may also extract the chemical components from solid or liquid sample matrices. The sample is injected into the GC inlet (Figure 1 (3)) through a septum which enables the injection of the sample mixture without losing the mobile phase. Connected to the inlet is the analytical column (Figure 1 (4)), a long (10 – 150 m), narrow (0.1 – 0.53 mm internal diameter) fused silica or metal tube which contains the stationary phase coated on the inside walls. The analytical column is held in the column oven which is heated during the analysis to elute the less volatile components. The outlet of the column is inserted into the detector (Figure 1 (5)) which responds to the chemical components eluting from the column to produce a signal. The signal is recorded by the acquisition software on a computer to produce a chromatogram (Figure 1 (6)).

Figure 1: A simplified diagram of a gas chromatograph showing: (1) carrier gas, (2) autosampler, (3) inlet, (4) analytical column, (5) detector and (6) / Un diagramma semplificato di un gascromatografo che mostra: (1) gas di trasporto, (2) autocampionatore, (3) ingresso, (4) colonna analitica, (5) rivelatore e (6) PC. Credit: Anthias Consulting.
After injection into the GC inlet, the chemical components of the sample mixture are first vaporized, if they aren’t already in the gas phase. For low concentration samples the whole vapour cloud is transferred into the analytical column by the carrier gas in what is known as splitless mode. For high concentration samples only a portion of the sample is transferred to the analytical column in split mode, the remainder is flushed from the system through the split line to prevent overloading of the analytical column.
Once in the analytical column, the sample components are separated by their different interactions with the stationary phase. Therefore, when selecting the type of column to use, the volatility and functional groups of the analytes should be considered to match them to the stationary phase. Liquid stationary phases mainly fall into two types: polyethylene glycol (PEG) or polydimethylsiloxane (PDMS) based, the latter with varying percentages of dimethyl, diphenyl or mid-polar functional groups, for example cyanopropylphenyl. Like separates like, therefore non-polar columns with dimethyl or a low percentage of diphenyl are good for separating non-polar analytes. Those molecules capable of π-π interactions can be separated on stationary phases containing phenyl groups. Those capable of hydrogen bonding, for example acids and alcohols, are best separated with PEG columns, unless they have undergone derivatization to make them less polar.
The final step is the detection of the analyte molecules when they elute from the column. There are many types of GC detectors, for example: those that respond to C-H bonds like the flame ionization detector (FID); those that respond to specific elements for example sulfur, nitrogen or phosphorus; and those that respond to specific properties of the molecule, like the ability to capture an electron, as is used with the electron capture detector (ECD).
Adding mass spectrometry to gas chromatography (GC-MS)
Mass spectrometry (MS) is an analytical technique that can be hyphenated to a GC and used instead of the GC detector. The neutral molecules elute from the analytical column and are ionised in the ion source to produce molecular ions which can degrade into fragment ions. The fragment and molecular ions are then separated in the mass analyser by their mass:charge (m/z) ratio and are detected. Data from a GC-MS is three dimensional, providing mass spectra that can be used for identity confirmation, to identify unknown analytes and to determine structural and chemical properties of molecules, as well as the chromatogram that can be used for qualitative and quantitative analysis.
How do you read a chromatogram and what does it tell you?
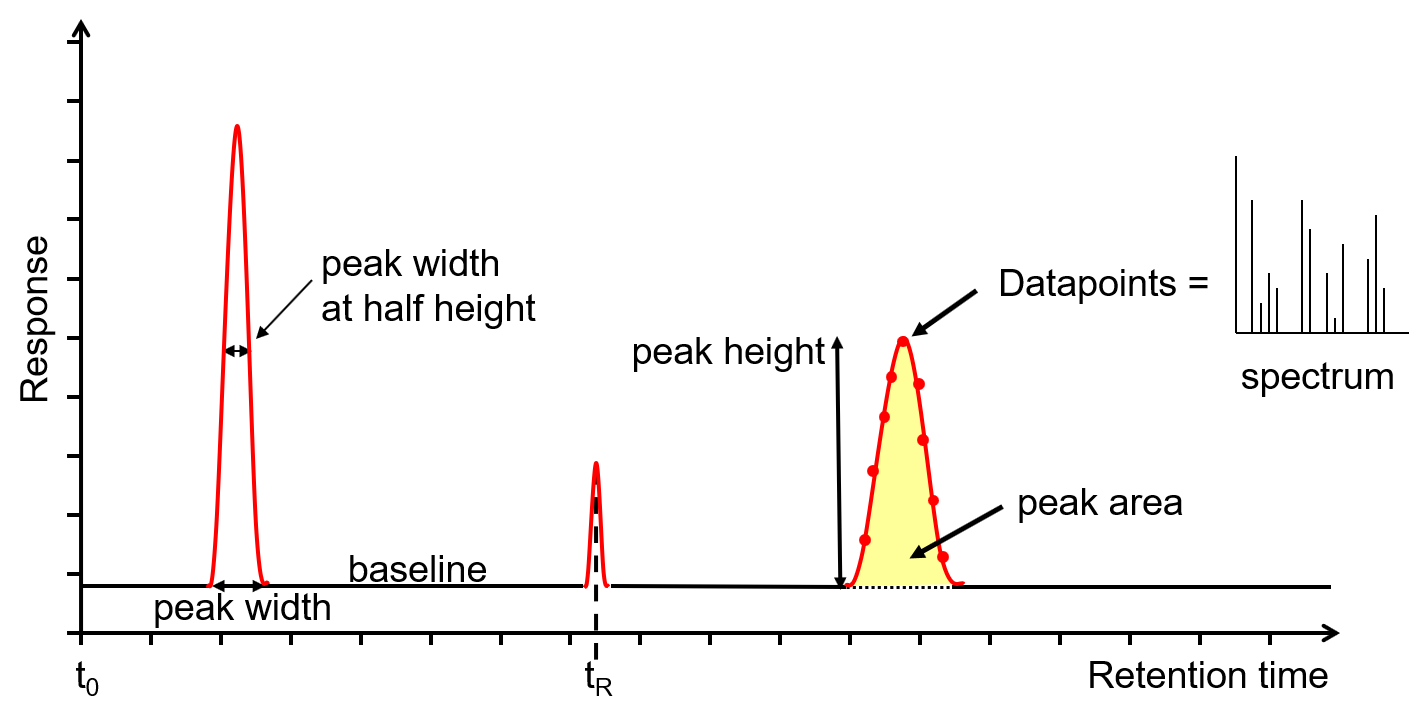
Figure 2: Chromatogram output from a GC or GC-MS. / Uscita cromatografica da un GC o GC-MS. Credit: Anthias Consulting.
The x-axis is the retention time, taken from the time the sample was injected into the GC (t0) to the end of the GC run. Each analyte peak has a retention time measured from the apex of the peak, for example tR. The y-axis is the measured response of the analyte peak in the detector. The baseline shows the signal from the detector when no analyte is eluting from the column, or it is below the detection limit. The baseline response is a mix of electrical noise (usually low) and chemical noise, such as impurities in the carrier gas, column stationary phase bleed and system contamination. Hence, if the baseline is higher than it should be, it is an indication of a problem or that maintenance is required. Various measurements can be taken from the peak, such as width at the baseline, width at half height, total height and area. The latter two are proportional to the concentration, however it is the area that is used for quantitation as it is less affected by band broadening. The measurements can be used to calculate the extent of band broadening, the spread of the analyte molecules on the column. Narrower, sharper peaks give better sensitivity (signal to noise ratio) and better resolution (peak separation). The peaks shown are Gaussian, however peak tailing (the right side of the peak is wider) indicates activity or a dead volume in the system, whereas a peak fronting (the left side of the peak is wider) indicates the column is overloaded. Accurate measurements are affected by the number of data points across a peak, with an ideal number being 15-25. Too few, makes the peak look like a child’s join-the-dots drawing, affecting peak area, resolution and, with GC-MS, deconvolution. Too many reduces the signal to noise, reducing sensitivity. For GC-MS data, each data point is a mass spectrum, the third dimension of data.
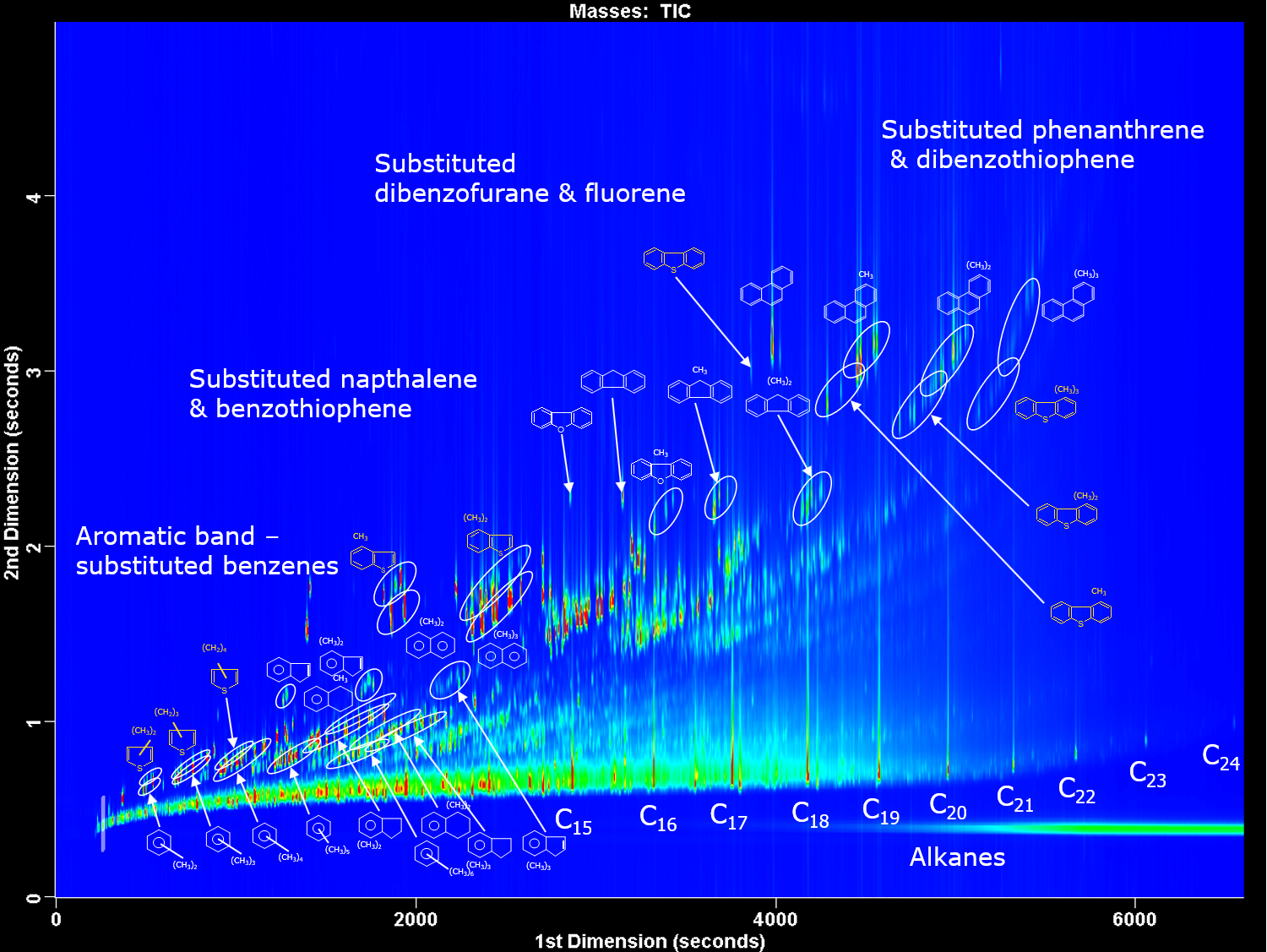
Figure 3: GC x GC contour plot of diesel showing the different chemical classes separated. 1st dimension column is non-polar and 2nd dimension column is mid-polar. / GC x GC grafico di contorno del diesel che mostra le diverse classi chimiche separate. La colonna di prima dimensione non è polare e la colonna di seconda dimensione è a metà polare. Credit: Anthias Consulting.
For complex samples where there are frequent coelutions, comprehensive two-dimensional chromatography (GC x GC) is used. Two columns, containing different stationary phases and therefore different separation mechanisms, are set-up in series. The “normal” set-up is a 1st dimension non-polar column followed by a 2nd dimension more polar column, as shown in Figure 3, for the analysis of diesel. A modulator is used between the two columns to take a cut from the first column and reinject in a narrow sample band onto the second column. Thermal modulators achieve this using temperature to trap and then release the molecules, flow modulators collect the effluent, compress and flush the molecules onto the second column. Cuts are taken throughout the run, usually every 1 to 10 seconds. Separation on the second column should be achieved before the next cut is introduced. This fast separation is achieved by using a short, narrow second column, usually 1-2 m of 0.1 mm internal diameter used with thermal modulators; or a short, wider second column, usually 5 m of 0.25 mm internal diameter used with flow modulators. GC x GC peaks are very narrow, down to 35 ms, therefore fast GC detectors or high acquisition rate mass spectrometers >100 Hz must be used to acquire enough data points.
Strengths and limitations of gas chromatography
GC is a widely used technique across most industries. It is used for routine analysis through to research, analysing a few to many hundreds (or thousands with GC x GC) of compounds in many different matrices, from solids to gases. It is a robust technique and is easily hyphenated to other techniques including mass spectrometry.
GC is limited to analysing volatile compounds from helium/hydrogen up to molecular weights of around 1250 u. Thermally labile compounds can degrade in a hot GC, therefore cold injection techniques and low temperatures should be used to minimize this. More polar analytes can become stuck or lost in the GC, therefore the system should be deactivated and well-maintained or these analytes derivatized.
Common problems with gas chromatography
The most common problem in GC is leaks. The mobile phase is a gas and flows throughout the system, therefore the correct installation of parts and consumables is important along with regular leak checking.
Activity is another issue for more polar analytes, especially those at trace levels. Silanol groups on the glass liners and column, and also a build-up of dirt in the system can cause tailing peaks, irreversible adsorption or catalytic breakdown. The inlet is the area that causes most problems as it is here the sample is injected, vaporized and transferred into the GC column. Therefore, regular inlet maintenance along with using the correct consumables, for example a deactivated inlet liner, is important to keep the instrument trouble-free.
ITALIANO
Cos'è la gascromatografia?
La gascromatografia (GC) è una tecnica analitica utilizzata per separare i componenti chimici di una miscela di campioni e quindi rilevarli per determinare la loro presenza o assenza e / o quanto è presente. Questi componenti chimici sono solitamente molecole o gas organici. Affinché GC abbia successo nella loro analisi, questi componenti devono essere volatili, di solito con un peso molecolare inferiore a 1250 Da e termicamente stabili in modo da non degradare nel sistema GC. GC è una tecnica ampiamente utilizzata in molti settori: per il controllo di qualità nella fabbricazione di molti prodotti, dalle automobili ai prodotti chimici, ai prodotti farmaceutici; a fini di ricerca dall'analisi dei meteoriti ai prodotti naturali; e per la sicurezza dall'ambiente, dal cibo alla medicina legale. I gascromatografi sono spesso sillabati in spettrometri di massa (GC-MS) per consentire l'identificazione dei componenti chimici.
Come funziona la gascromatografia?
Come suggerisce il nome, GC utilizza un gas vettore nella separazione, che svolge la parte della fase mobile (Figura 1 (1)). Il gas di trasporto trasporta le molecole del campione attraverso il sistema GC, idealmente senza reagire con il campione o danneggiare i componenti dello strumento.
Il campione viene prima introdotto nel gascromatografo (GC), con una siringa o trasferito da un autocampionatore (Figura 1 (2)) che può anche estrarre i componenti chimici da matrici di campioni solidi o liquidi. Il campione viene iniettato nell'ingresso GC (Figura 1 (3)) attraverso un setto che consente l'iniezione della miscela del campione senza perdere la fase mobile. All'ingresso è collegata la colonna analitica (Figura 1 (4)), un tubo di silice o metallo fuso lungo (10-150 m), stretto (0,1 - 0,53 mm di diametro interno) che contiene la fase stazionaria rivestita sulle pareti interne. La colonna analitica viene mantenuta nel forno a colonna che viene riscaldato durante l'analisi per eluire i componenti meno volatili. L'uscita della colonna viene inserita nel rivelatore (Figura 1 (5)) che risponde ai componenti chimici che eluiscono dalla colonna per produrre un segnale. Il segnale viene registrato dal software di acquisizione su un computer per produrre un cromatogramma (Figura 1 (6)).
Dopo l'iniezione nell'ingresso GC, i componenti chimici della miscela campione vengono prima vaporizzati, se non sono già in fase gassosa. Per campioni a bassa concentrazione, l'intera nube di vapore viene trasferita nella colonna analitica dal gas vettore in quella che è nota come modalità splitless. Per i campioni ad alta concentrazione, solo una parte del campione viene trasferita alla colonna analitica in modalità split, il resto viene scaricato dal sistema attraverso la linea di split per evitare il sovraccarico della colonna analitica.
Una volta nella colonna analitica, i componenti del campione sono separati dalle loro diverse interazioni con la fase stazionaria. Pertanto, quando si seleziona il tipo di colonna da utilizzare, è necessario considerare la volatilità e i gruppi funzionali degli analiti per farli corrispondere alla fase stazionaria. Le fasi stazionarie liquide si dividono principalmente in due tipi: polietilenglicole (PEG) o polidimetilsilossano (PDMS), quest'ultimo con percentuali variabili di gruppi funzionali dimetilici, difenilici o polari, ad esempio cianopropilfenile. Come il simile separa simile, quindi le colonne non polari con dimetile o una bassa percentuale di difenile sono buone per separare gli analiti non polari. Quelle molecole capaci di interazioni π-π possono essere separate su fasi stazionarie contenenti gruppi fenilici. Quelli in grado di legare l'idrogeno, ad esempio acidi e alcoli, sono meglio separati con colonne PEG, a meno che non siano stati sottoposti a derivatizzazione per renderli meno polari.
Il passaggio finale è il rilevamento delle molecole dell'analita quando eluiscono dalla colonna. Esistono molti tipi di rivelatori GC, ad esempio: quelli che rispondono ai legami C-H come il rivelatore a ionizzazione di fiamma (FID); quelli che rispondono a elementi specifici come ad esempio zolfo, azoto o fosforo; e quelli che rispondono a proprietà specifiche della molecola, come la capacità di catturare un elettrone, come viene usato con il rivelatore di cattura di elettroni (ECD).
Aggiunta di spettrometria di massa alla gascromatografia (GC-MS)
La spettrometria di massa (MS) è una tecnica analitica che può essere sillabata in un GC e utilizzata al posto del rivelatore GC. Le molecole neutre eluiscono dalla colonna analitica e sono ionizzate nella sorgente ionica per produrre ioni molecolari che possono degradare in ioni frammento. Il frammento e gli ioni molecolari vengono quindi separati nell'analizzatore di massa dal loro rapporto massa: carica (m / z) e vengono rilevati. I dati di un GC-MS sono tridimensionali e forniscono spettri di massa che possono essere utilizzati per la conferma dell'identità, per identificare analiti sconosciuti e per determinare le proprietà strutturali e chimiche delle molecole, nonché il cromatogramma che può essere utilizzato per analisi qualitative e quantitative.
Come leggi un cromatogramma e cosa ti dice?
L'asse x è il tempo di ritenzione, preso dal momento in cui il campione è stato iniettato nel GC (t0) fino alla fine della corsa del GC. Ogni picco di analita ha un tempo di ritenzione misurato dall'apice del picco, ad esempio tR. L'asse y è la risposta misurata del picco dell'analita nel rivelatore. La linea di base mostra il segnale dal rivelatore quando nessun analita viene eluito dalla colonna o è al di sotto del limite di rilevazione. La risposta di base è un mix di rumore elettrico (generalmente basso) e rumore chimico, come impurità nel gas di trasporto, spurgo di fase stazionario della colonna e contaminazione del sistema. Quindi, se la linea di base è più alta di quanto dovrebbe essere, è un'indicazione di un problema o della necessità di manutenzione. Diverse misure possono essere prese dal picco, come larghezza alla linea di base, larghezza a mezza altezza, altezza totale e area. Gli ultimi due sono proporzionali alla concentrazione, tuttavia è l'area che viene utilizzata per la quantificazione in quanto è meno influenzata dall'ampliamento della banda. Le misure possono essere utilizzate per calcolare l'estensione dell'ampliamento della banda, la diffusione delle molecole dell'analita sulla colonna. I picchi più stretti e più nitidi offrono una migliore sensibilità (rapporto segnale-rumore) e una migliore risoluzione (separazione dei picchi). I picchi mostrati sono gaussiani, tuttavia il picco di coda (il lato destro del picco è più largo) indica l'attività o un volume morto nel sistema, mentre un fronte di picco (il lato sinistro del picco è più largo) indica che la colonna è sovraccarica. Misurazioni accurate sono influenzate dal numero di punti dati attraverso un picco, con un numero ideale compreso tra 15 e 25. Troppo pochi, fanno apparire il picco come un disegno a punti uniti di un bambino, influenzando l'area del picco, la risoluzione e, con GC-MS, la deconvoluzione. Troppi riducono il segnale in rumore, riducendo la sensibilità. Per i dati GC-MS, ogni punto dati è uno spettro di massa, la terza dimensione dei dati.
Per campioni complessi in cui vi sono frequenti coeluzioni, viene utilizzata la cromatografia bidimensionale completa (GC x GC). Due colonne, contenenti diverse fasi stazionarie e quindi diversi meccanismi di separazione, sono disposte in serie. Il set-up “normale” è una colonna non polare di 1a dimensione seguita da una colonna più polare di 2a dimensione, come mostrato nella Figura 3, per l'analisi del diesel. Un modulatore viene utilizzato tra le due colonne per eseguire un taglio dalla prima colonna e reintegrarlo in una stretta banda di campionamento sulla seconda colonna. I modulatori termici ottengono questo utilizzando la temperatura per intrappolare e quindi rilasciare le molecole, i modulatori di flusso raccolgono l'effluente, comprimono e sciacquano le molecole sulla seconda colonna. I tagli vengono effettuati durante la corsa, di solito ogni 1 a 10 secondi. La separazione sulla seconda colonna dovrebbe essere ottenuta prima dell'introduzione del taglio successivo. Questa rapida separazione si ottiene utilizzando una seconda colonna corta e stretta, generalmente 1-2 m di diametro interno di 0,1 mm utilizzato con i modulatori termici; o una seconda colonna più corta e più larga, generalmente 5 m di diametro interno di 0,25 mm utilizzato con i modulatori di flusso. I picchi GC x GC sono molto stretti, fino a 35 ms, pertanto è necessario utilizzare rilevatori GC veloci o spettrometri di massa ad alta velocità di acquisizione> 100 Hz per acquisire punti dati sufficienti.
Punti di forza e limiti della gascromatografia
GC è una tecnica ampiamente utilizzata nella maggior parte dei settori. È usato per analisi di routine fino alla ricerca, analizzando da poche a molte centinaia (o migliaia con GC x GC) di composti in molte matrici diverse, dai solidi ai gas. È una tecnica robusta ed è facilmente sillabata ad altre tecniche tra cui la spettrometria di massa.
Il GC si limita ad analizzare composti volatili da elio / idrogeno fino a pesi molecolari di circa 1250 u. I composti termicamente labili possono degradarsi in un GC caldo, pertanto per ridurre al minimo questa tecnica è necessario utilizzare tecniche di iniezione a freddo e basse temperature. Un numero maggiore di analiti polari può rimanere bloccato o perso nel GC, pertanto il sistema deve essere disattivato e ben mantenuto o derivato da questi analiti.
Problemi comuni con la gascromatografia
Il problema più comune in GC sono le perdite. La fase mobile è un gas e fluisce attraverso il sistema, quindi la corretta installazione di parti e materiali di consumo è importante insieme a un controllo periodico delle perdite.
L'attività è un altro problema per più analiti polari, in particolare quelli a livello di tracce. I gruppi di silanolo sui rivestimenti di vetro e sulla colonna, nonché un accumulo di sporcizia nel sistema possono causare picchi di scodamento, adsorbimento irreversibile o rottura catalitica. L'ingresso è l'area che causa la maggior parte dei problemi in quanto è qui che il campione viene iniettato, vaporizzato e trasferito nella colonna GC. Pertanto, una manutenzione regolare dell'iniettore e l'utilizzo di materiali di consumo corretti, ad esempio un rivestimento dell'iniettore disattivato, sono importanti per mantenere lo strumento senza problemi.
Da:



Commenti
Posta un commento