Harnessing the Power of In Vitro Antibody Selection from Libraries / Sfruttare il potere della selezione di anticorpi in vitro dalle biblioteche
Harnessing the Power of In Vitro Antibody Selection from Libraries / Sfruttare il potere della selezione di anticorpi in vitro dalle biblioteche
The recently published recommendations of the European Commission Joint Research Centre (JRC) shine a spotlight on the versatility and scientific benefits of universal antibody libraries in combination with selection technologies, such as phage display, in generating precision antibodies for biomedical and scientific use. The JRC Science for Policy Report reveals a need for broader understanding across the scientific community of the disadvantages of animal-derived antibodies in terms of reproducibility, specificity, and flexibility, and challenges the widely held historical belief that animals are the only source for novel antibodies.
The report documents the findings of the European Union Reference Laboratory for Alternatives to Animal Testing (EURL ECVAM), which has a mandate, granted by EU legislation, to ensure the protection of animals used for scientific purposes. The EURL ECVAM explains that, aside from the ethical concerns associated with the use of animal-based techniques when alternative methodologies exist, the reliability of animal-derived antibodies is known to be often seriously flawed. In contrast, non-animal-derived molecular antibody tools offer greater precision, reproducibility, and flexibility.
The review states that animals should no longer be used for the development and production of antibodies for research, regulatory, diagnostic, and therapeutic applications. Instead, large antibody libraries and in vitro selection methods should be leveraged to address the shortcomings of conventional animal-based approaches.
The current situation
Despite the widely acknowledged drawbacks associated with traditional antibody generation techniques (for example, time-consuming protocols, quality issues, and poor reproducibility), polyclonal and monoclonal antibodies are still made by immunization of laboratory animals. Methods used to generate animal-based antibodies have not improved significantly over recent decades. Problems associated with lack of renewability and specificity, unknown genetic sequences, and the loss of hybridomas for monoclonal antibodies result in significant and costly wastage of materials and time. There is a general acceptance across the scientific field of the intrinsic limitations associated with animal-based antibodies. The JCR report creates a demand for scientifically superior resources.
Many non-animal-derived antibodies are already approved in Europe and the United States for use in therapeutics and diagnostics, and many thousands have been generated as research reagents. Indeed, academia and biotechnology companies have developed precision antibody products from non-animal sources for more than 25 years, some of which are widely commercially available and have been well characterized and validated in applications.
Leveraging existing expertise and established technologies
The JCR report recognizes the vast and robust body of evidence supporting the use of non-animal-derived affinity reagents as well as the practical advantages that these products offer concerning consistency and reproducibility. Laboratory-based techniques allow protocols for the generation of antibodies and antibody fragments to be standardized, refined, and optimized.
Universal antibody libraries were developed approximately 30 years ago and have been improved over time. Large libraries provide multiple benefits, including high success rates and rapid antibody generation. For example, the fully synthetic Human Combinatorial Antibody Libraries (HuCAL®) phage library, used by Bio-Rad Laboratories to generate recombinant antibodies for research and diagnostics and for the company’s catalog products and custom service offerings, contains 45 billion functional human antibody genes in Fab format.
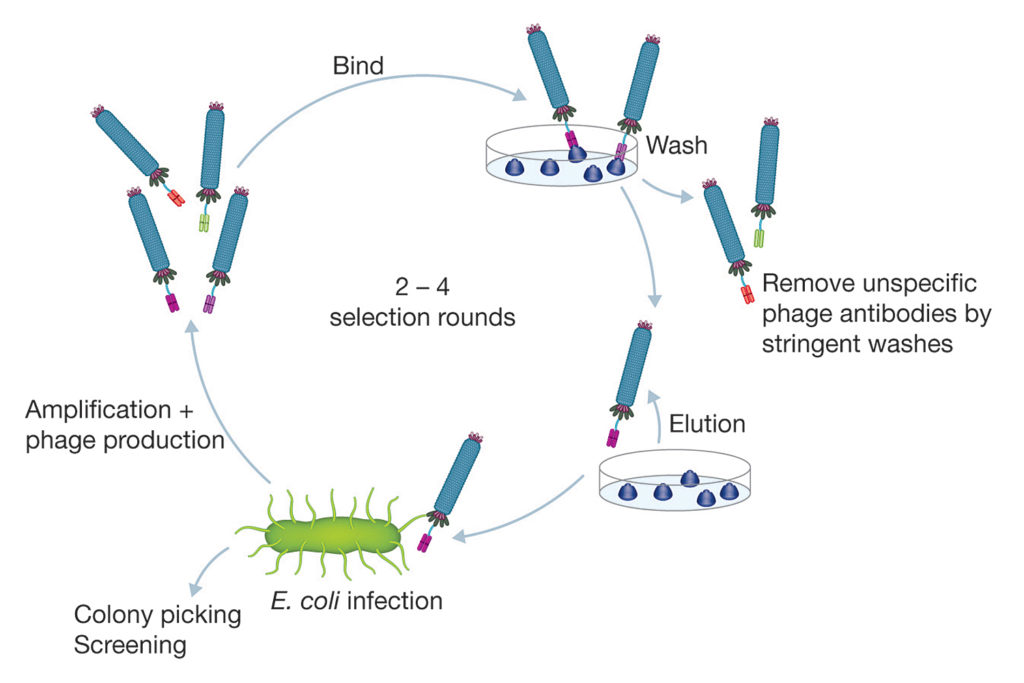
The JCR report recommends the use of guided in vitro techniques for selection of antibody sequences defined by essential characteristics (for example, stability and cross-reactivity). As the most mature technology in this field, phage display is already widely used and capable of efficiently generating a near-infinite range of high-quality antibodies from such libraries (Figure 1). Antibodies generated through phage display libraries may be developmentally, functionally, and structurally equivalent to those produced by animals, and improvements can be made to elevate quality further by refining or adapting the resulting gene sequences.
Universal libraries and in vitro selection strategies offer a powerful combination, enabling isolation of antibodies against virtually any type of antigen. These may include low immunogenic or “self” antigens and toxins, or antibodies with the ability to differentiate between two subtly different proteins. The resulting recombinant antibodies can be further engineered to offer the flexibility of different formats, such as Fab and bivalent Fab, constructs that may incorporate a variety of detection and purification tags, and full-length immunoglobulins of any isotype. They can also be further engineered to gain incremental improvements in terms of binding affinity by molecular evolution.
The JCR report states that a universal recombinant library can produce a diversity of antibody candidates equivalent to a lifetime supply of animals. Indeed, it is easy to see how the use of bench-based methods can offer considerable economic, resource, and time efficiencies when compared with the cost of ongoing animal care, immunization, and antibody purification procedures—in addition to the frequent losses due to low product yield or low quality associated with polyclonal sera or hybridoma cells. Protocols that use synthetic libraries and phage display selection platforms allow rapid generation and screening of novel antibodies in a matter of weeks, whereas animal-based methods take many months to complete.
A look to the future
If stakeholders in the scientific community step away from the widespread use of animals to generate affinity reagents, the resulting increase in demand for non-animal-derived products will drive further technological enhancements and innovations in this arena.
Evolving proprietary phage display systems are already bringing new possibilities and enabling antibody selection processes to be simplified and streamlined. For example, the CysDisplay® proprietary platform uses an engineered disulfide bridge to link antibody fragments to a phage protein, allowing elution through the addition of a reducing agent, rather than relying on traditional affinity-dependent approaches (Figure 2). This feature allows for better automation and retrieval of very high-affinity clones. Advances in protein ligation technologies have seen sophisticated molecular tagging tools being incorporated into recombinant antibodies, such as the SpyTag/SpyCatcher system, that circumvent cloning steps or facilitate antibody site-directed conjugation.
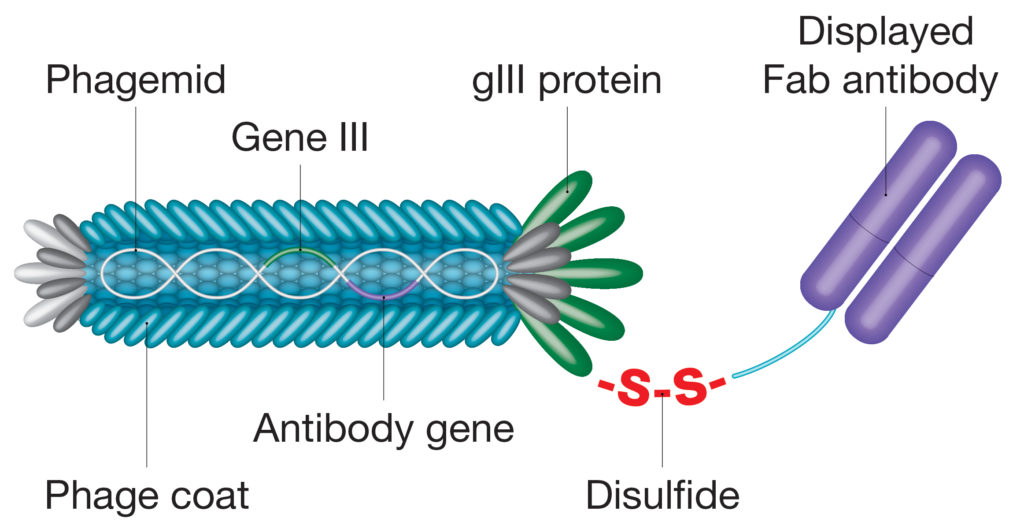
Figure 2. CysDisplay technology: a proprietary form of phage display featuring the surface display of an antibody fragment on filamentous phage via a cleavable disulfide bond / Tecnologia CysDisplay: una forma proprietaria di visualizzazione dei fagi che mostra la visualizzazione della superficie di un frammento di anticorpo sul fago filamentoso tramite un legame disolfuro scindibile
Moving forward, existing, well-characterized monoclonal antibodies from hybridomas should be sequenced and produced using recombinant systems. To tackle the issues associated with the production of polyclonal antibodies, the EURL ECVAM panel recommends laboratory-based methods that generate defined combinations of recombinant antibodies (or “multiclonal” antibodies) from universal phage display libraries. This has the potential to combine the advantages of polyclonal antibodies (in terms of multiepitope binding and improved sensitivity) with the consistency of recombinant antibodies, and to provide a renewable resource.
A call to action
The JCR report concludes with a call for greater education, training, and awareness concerning the potential of non-animal-derived antibodies. Activities should focus on easing access to reagents and communication of case studies that emphasize the quality of these products. This needs to be driven by government authorities, funding agencies, and publishers through the setting of higher scientific, regulatory, and ethical standards. All funding applications or scientific manuscripts detailing newly generated antibodies should use non-animal-derived materials from naïve universal or engineered library sources that are defined at the sequence level. Grant requests and scientific reports proposing the use of antibodies generated through animal immunization should be challenged.
Academic institutions are urged to coordinate efforts to establish non-animal-derived libraries and broader access to services that will support research activities. The report signposts those manufacturers already leading the way in offering non-animal-derived antibodies in their catalogs.
The message is clear: through the harnessing of non-animal-based affinity products and technologies, we can make significant advances in safeguarding the welfare of millions of animals, while raising scientific standards concerning the use of antibody products in research, diagnostics, and therapeutics.
ITALIANO
Le raccomandazioni pubblicate di recente dal Centro comune di ricerca (JRC) della Commissione europea puntano i riflettori sulla versatilità e sui vantaggi scientifici delle librerie di anticorpi universali in combinazione con le tecnologie di selezione, come la visualizzazione dei fagi, nella generazione di anticorpi di precisione per uso biomedico e scientifico. Il rapporto del JRC Science for Policy rivela la necessità di una più ampia comprensione nella comunità scientifica degli svantaggi degli anticorpi di origine animale in termini di riproducibilità, specificità e flessibilità, e sfida la convinzione storica ampiamente diffusa che gli animali siano l'unica fonte di nuovi anticorpi.
Il rapporto documenta i risultati del Laboratorio di riferimento dell'Unione europea per le alternative alla sperimentazione animale (EURL ECVAM), che ha il mandato, concesso dalla legislazione dell'UE, di garantire la protezione degli animali utilizzati a fini scientifici. L'ECVAM EURL spiega che, a parte le preoccupazioni etiche associate all'uso di tecniche basate su animali quando esistono metodologie alternative, è noto che l'affidabilità degli anticorpi di origine animale è spesso gravemente viziata. Al contrario, gli strumenti di anticorpi molecolari non di origine animale offrono maggiore precisione, riproducibilità e flessibilità.
La revisione afferma che gli animali non dovrebbero più essere utilizzati per lo sviluppo e la produzione di anticorpi per applicazioni di ricerca, regolatorie, diagnostiche e terapeutiche. Invece, grandi librerie di anticorpi e metodi di selezione in vitro dovrebbero essere sfruttati per affrontare le carenze degli approcci convenzionali basati sugli animali.
La situazione attuale
Nonostante gli svantaggi ampiamente riconosciuti associati alle tecniche tradizionali di generazione di anticorpi (ad esempio protocolli che richiedono molto tempo, problemi di qualità e scarsa riproducibilità), gli immunogeni policlonali e monoclonali sono ancora prodotti dall'immunizzazione di animali da laboratorio. I metodi utilizzati per generare anticorpi di origine animale non sono migliorati in modo significativo negli ultimi decenni. I problemi associati alla mancanza di rinnovabilità e specificità, sequenze genetiche sconosciute e la perdita di ibridomi per gli anticorpi monoclonali comportano uno spreco significativo e costoso di materiali e tempo. Esiste un'accettazione generale in tutto il campo scientifico delle limitazioni intrinseche associate all'animale. anticorpi a base. Il rapporto JCR crea una richiesta di risorse scientificamente superiori.
Molti anticorpi non di origine animale sono già approvati in Europa e negli Stati Uniti per l'uso in terapia e diagnostica e molte migliaia sono stati generati come reagenti di ricerca. Infatti, il mondo accademico e le società di biotecnologia hanno sviluppato prodotti anticorpali di precisione da fonti non animali per più di 25 anni, alcuni dei quali sono ampiamente disponibili in commercio e sono stati ben caratterizzati e convalidati nelle applicazioni.
Sfruttando le competenze esistenti e le tecnologie consolidate
Il rapporto JCR riconosce la vasta e solida serie di prove a sostegno dell'uso di reagenti di affinità non derivati da animali, nonché i vantaggi pratici che questi prodotti offrono in termini di coerenza e riproducibilità. Le tecniche di laboratorio consentono di standardizzare, perfezionare e ottimizzare i protocolli per la generazione di anticorpi e frammenti di anticorpi.
Le librerie di anticorpi universali sono state sviluppate circa 30 anni fa e sono state migliorate nel tempo. Le librerie di grandi dimensioni offrono molteplici vantaggi, inclusi tassi di successo elevati e rapida generazione di anticorpi. Ad esempio, la libreria dei fagi completamente sintetici Human Combinatorial Antibody Libraries (HuCAL®), utilizzata da Bio-Rad Laboratories per generare anticorpi ricombinanti per la ricerca e la diagnostica e per i prodotti del catalogo dell'azienda e le offerte di servizi personalizzati, contiene 45 miliardi di geni funzionali di anticorpi umani in Formato favoloso
Il rapporto JCR raccomanda l'uso di tecniche guidate in vitro per la selezione di sequenze di anticorpi definite da caratteristiche essenziali (ad esempio stabilità e reattività crociata). Essendo la tecnologia più matura in questo campo, la visualizzazione dei fagi è già ampiamente utilizzata e in grado di generare in modo efficiente una gamma quasi infinita di anticorpi di alta qualità da tali librerie (Figura 1). Gli anticorpi generati attraverso le librerie di visualizzazione dei fagi possono essere evolutivamente, funzionalmente e strutturalmente equivalenti a quelli prodotti dagli animali, e possono essere apportati miglioramenti per elevare ulteriormente la qualità raffinando o adattando le sequenze geniche risultanti.
Le biblioteche universali e le strategie di selezione in vitro offrono una potente combinazione che consente l'isolamento di anticorpi praticamente da qualsiasi tipo di antigene. Questi possono includere antigeni e tossine immunogenici o "auto" bassi o anticorpi con la capacità di differenziare tra due proteine sottilmente diverse. Gli anticorpi ricombinanti risultanti possono essere ulteriormente progettati per offrire la flessibilità di diversi formati, come Fab e Fab bivalente, costrutti che possono incorporare una varietà di tag di rilevazione e purificazione e immunoglobuline a lunghezza intera di qualsiasi isotipo. Possono anche essere ulteriormente ingegnerizzati per ottenere miglioramenti incrementali in termini di affinità di legame per evoluzione molecolare.
Il rapporto JCR afferma che una libreria ricombinante universale può produrre una varietà di candidati anticorpali equivalenti a una fornitura a vita di animali. In effetti, è facile vedere come l'uso di metodi basati su banco possa offrire considerevoli efficienze economiche, di risorse e di tempo rispetto ai costi delle attuali procedure di cura degli animali, immunizzazione e purificazione degli anticorpi, oltre alle frequenti perdite dovute a bassa resa del prodotto o bassa qualità associata a sieri policlonali o cellule di ibridoma. I protocolli che utilizzano librerie sintetiche e piattaforme di selezione del fago consentono la generazione e lo screening rapidi di nuovi anticorpi nel giro di poche settimane, mentre i metodi basati su animali richiedono molti mesi per essere completati.
Uno sguardo al futuro
Se le parti interessate nella comunità scientifica si allontanano dall'uso diffuso di animali per generare reagenti di affinità, il conseguente aumento della domanda di prodotti non di origine animale guiderà ulteriori miglioramenti tecnologici e innovazioni in questo campo.
I sistemi di visualizzazione dei fagi proprietari in continua evoluzione stanno già offrendo nuove possibilità e semplificando e semplificando i processi di selezione degli anticorpi. Ad esempio, la piattaforma proprietaria CysDisplay® utilizza un ponte disolfuro ingegnerizzato per collegare i frammenti di anticorpi a una proteina fagica, consentendo l'eluizione attraverso l'aggiunta di un agente riducente, piuttosto che fare affidamento sui tradizionali approcci dipendenti dall'affinità (Figura 2) . Questa caratteristica consente per una migliore automazione e recupero di cloni ad altissima affinità. I progressi nelle tecnologie di legatura delle proteine hanno visto l'incorporazione di sofisticati strumenti di marcatura molecolare negli anticorpi ricombinanti, come il sistema SpyTag / SpyCatcher, che aggirano le fasi di clonazione o facilitano la coniugazione diretta al sito dell'anticorpo.
Andando avanti, gli anticorpi monoclonali esistenti e ben caratterizzati da ibridomi dovrebbero essere sequenziati e prodotti utilizzando sistemi ricombinanti. Per affrontare i problemi associati alla produzione di anticorpi policlonali, il pannello EURL ECVAM raccomanda metodi di laboratorio che generano combinazioni definite di anticorpi ricombinanti (o anticorpi "multiclonali") da librerie universali di visualizzazione dei fagi. Questo ha il potenziale per combinare i vantaggi degli anticorpi policlonali (in termini di legame multiepitopico e migliore sensibilità) con la consistenza degli anticorpi ricombinanti e di fornire una risorsa rinnovabile.
Un invito all'azione
Il rapporto JCR si conclude con una richiesta di maggiore istruzione, formazione e consapevolezza riguardo al potenziale degli anticorpi non di origine animale. Le attività dovrebbero concentrarsi sulla facilitazione dell'accesso ai reagenti e sulla comunicazione di casi di studio che enfatizzano la qualità di questi prodotti. Ciò deve essere guidato dalle autorità governative, dalle agenzie di finanziamento e dagli editori attraverso la definizione di standard scientifici, normativi ed etici più elevati. Tutte le domande di finanziamento o i manoscritti scientifici che descrivono in dettaglio gli anticorpi di nuova generazione devono utilizzare materiali non derivati da animali da fonti bibliotecarie ingenue universali o ingegnerizzate che sono definite a livello di sequenza. Le richieste di sovvenzioni e le relazioni scientifiche che propongono l'uso di anticorpi generati attraverso l'immunizzazione degli animali dovrebbero essere contestate.
Le istituzioni accademiche sono invitate a coordinare gli sforzi per istituire biblioteche non di origine animale e un più ampio accesso ai servizi a sostegno delle attività di ricerca. Il rapporto indica quei produttori che sono già all'avanguardia nell'offerta di anticorpi non di origine animale nei loro cataloghi.
Il messaggio è chiaro: attraverso lo sfruttamento di prodotti e tecnologie di affinità non di origine animale, possiamo fare progressi significativi nella salvaguardia del benessere di milioni di animali, elevando al contempo gli standard scientifici riguardanti l'uso di prodotti anticorpali nella ricerca, nella diagnostica e nella terapia. .
Da:



Commenti
Posta un commento